< sve vesti
Rani intenzivni VS eskalacioni pristup: desetogodišnji uticaj na onesposobljenost kod relapsne multiple skleroze
05. avgust 2025.
Multipla skleroza (MS) je hronična autoimuna bolest centralnog nervnog sistema, koju karakterišu različiti patološki mehanizmi koji čine kontinuum neuroinflamacije i neurodegeneracije. (1–3). Akumulacija neurološke onesposobljenosti tokom vremena, većim delom kao posledica subkliničke aktivnosti bolesti i progresije nezavisne od relapsne aktivnosti (PIRA), trenutno je glavni terapijski izazov u lečenju multiple skleroze. (4, 5). Smanjenjem stope relapsa i ograničavanjem progresije onesposobljenosti, terapije koje modifikuju prirodni tok bolesti (DMT) drastično su promenile lečenje multiple skleroze tokom poslednjih nekoliko godina (6).
U poređenju sa umereno efikasnim (ME) terapijama, lečenje visoko efikasnim (HE) DMT terapijama pokazalo se korisnijim u smanjenju akumulacije oštećenja uzrokovanog pogoršanjem povezanim sa relapsnom aktivnosti (RAW) i PIRA fenomenom. (4, 7) Ipak, odluka o ranom započinjanju HE-DMT terapija (rani intenzivni tretman, EIT) ili ostavljanju ovih terapija za eskalaciju (ESK) nakon neuspeha umereno efikasnih terapija (ME) ostaje predmet debate. (8). Da bi se optimizovali dugoročni ishodi i uticaj na onesposobljenost, strategije rane intenzivne terapije EIT su ključne i preporučuje ih sve veći broj novijih opservacionih studija i stručnih mišljenja. (9, 10)
Studija autora Pietro Iaffaldano i kolega ( 11) je imala za cilj da ispita desetogodišnji uticaj rane intenzivne terapije (EIT) u poređenju sa eskalacionim pristupom (ESC) na tok invaliditeta tokom vremena. i da proceni vreme do prve potvrđene akumulacije onesposobljenosti u trajanju od šest meseci (CDA), progresije nezavisne od relapsa (PIRA) i pogoršanja povezanih sa relapsom (RAW), u velikoj kohorti pacijenata sa relapsno-remitentnom multiplom sklerozom (RMS) iz italijanskog registra za MS i srodne poremećaje (I-MS&RD). (12).
Ova opservaciona studija obuhvatila je 4878 pacijenata sa RMS iz italijanskog registra za multiplu sklerozu. Učesnici koji su ispunjavali kriterijume započeli su svoju prvu terapiju koja modifikuje tok bolesti (DMT) u roku od 3 godine od početka bolesti i imali su ≥5 godina praćenja sa najmanje tri procene na EDSS skali. Pacijenti su kategorisani u EIT grupu ako su započeli sa HE-DMT terapijom i u ESC grupu ako su HE-DMT terapije započete nakon ≥1 godine terapije umerene efikasnosti. Usklađivanje rezultata (propensity score matching) je sprovedeno kako bi se uravnotežile početne karakteristike.
Ishodi su obuhvatali tokove onesposobljenosti procenjene korišćenjem linearnih mešovitih modela za ponovljena merenja, kao i rizike od potvrđenog nagomilavanja invaliditeta (CDA), progresije nezavisne od aktivnosti relapsa (PIRA) i pogoršanja povezanog sa relapsom (RAW), koji su procenjeni korišćenjem Koksovih modela proporcionalnih hazarda.
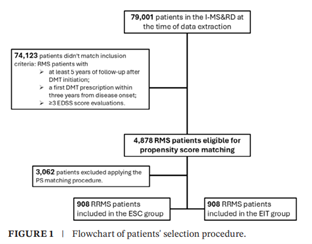
Klinički podaci za 79.001 pacijenta bili su dostupni u I-MS&RD registru u trenutku ekstrakcije podataka. Nakon primene kriterijuma za uključivanje, dobijena je kohorta od 4878 pacijenata sa RMS. Među njima, 914 pacijenata je lečeno prema EIT pristupu, dok je 3964 pacijenata pratilo ESC strategiju. Nakon primene postupka uparivanja po sklonosti (PS matching), za analizu je zadržano 908 parova pacijenata, čime je obezbeđena ravnoteža u početnim demografskim i kliničkim karakteristikama.
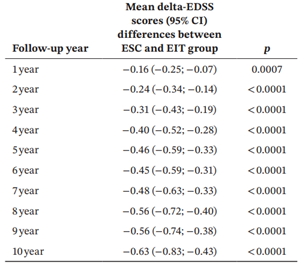
Longitudinalna analiza progresije onesposobljenosti pokazala je značajne razlike između dve strategije lečenja. Tabela 3 prikazuje prosečne procenjene razlike u delta-EDSS skoru sa odgovarajućim intervalima pouzdanosti za svaku godinu praćenja u upoređenim grupama. Procenjeni baseline EDSS iznosio je 2,52 (95% CI: 2,33–2,71) u ESC grupi i 2,45 (95% CI: 2,26–2,64) u EIT grupi. Tokom 10 godina praćenja, prosečne procenjene godišnje vrednosti delta-EDSS bile su značajno niže u EIT grupi (p < 0,05). Ukupna prosečna razlika u delta-EDSS između grupa iznosila je −0,16 (95% CI: −0,25 do −0,07; p = 0,0007), u korist EIT strategije. Ova razlika se postepeno povećavala tokom vremena, dostigavši −0,46 (95% CI: −0,59 do −0,33), čime se naglašava prednost za pacijente lečene prema EIT pristupu, i ta razlika je opstajala i rasla tokom perioda ispitivanja.
U ovoj kohorti EIT pristup je bio povezan sa nižim rizicima za CDA (p < 0,0001), PIRA (p = 0,0074) i RAW (p = 0,0021) događaje. Ovi rezultati su istakli superiornost EIT-a u poređenju sa ESC-om u razvoju dugoročne onesposobljenosti u RMS-u.
Nedavna studija iz registra I-MS&RD fokusirala se na pacijente sa prethodno nelečenom RRMS i pokazala je da HE-DMT kao što su Okrelizumab i Natalizumab snažno suzbijaju RAW događaje i imaju sličan uticaj na PIRA (13). Ovo je ključno, s obzirom na to da su pacijenti sa PIRA imali značajno strmiji porast EDSS rezultata nego oni bez PIRA (14).
Spelman i kolege su uporedili pacijente koji su započeli terapiju niske do umerene efikasnosti (LM DMT) sa onima koji su primali visoko efikasnu terapiju (HE-DMT) prve linije u studiji švedskog MS registra i zaključili da je grupa sa LM efikasnošću imala znatno veći neprilagođeni rizik od CDW događaja. HE-DMT grupa je takođe imala nižu stopu PIRA (15).
Zaključno, ovi rezultati iz registra I-MS&RD dodatno potvrđuju da rani početak visoko efikasne terapije (HE-DMT) smanjuje rizik od progresije onesposobljenosti i poboljšava dugoročne ishode kod pacijenata sa RMS u poređenju sa eskalacionom (ESC) strategijom, sa značajnim uticajem ranog intenzivnog lečenja (EIT) u smanjenju rizika od postizanja prvog PIRA događaja (11).
Reference:
- F. D. Lublin, D. A. Häring, H. Ganjgahi, et al., “How Patients With Multiple Sclerosis Acquire Disability,” Brain 145, no. 9 (2022): 3147–3161.
- T. Kuhlmann, M. Moccia, T. Coetzee, et al., “Multiple Sclerosis Progression: Time for a New Mechanism-Driven Framework,” Lancet Neurology 22, no. 1 (2023): 78–88
- M. Calabrese, P. Preziosa, A. Scalfari, et al., “Determinants and Biomarkers of Progression Independent of Relapses in Multiple Sclerosis,” Annals of Neurology 96, no. 1 (2024): 1–20.
- P. Iaffaldano, E. Portaccio, G. Lucisano, et al., “Multiple Sclerosis Progression and Relapse Activity in Children,” JAMA Neurology 81, no. 1 (2024): 88.
- E. Portaccio, M. Betti, E. De Meo, et al., “Progression Independent of Relapse Activity in Relapsing Multiple Sclerosis: Impact and Relationship With Secondary Progression,” Journal of Neurology 271, no. 8 (2024): 5074–5082.
- G. Comi, G. Dalla Costa, and L. Moiola, “Newly Approved Agents for Relapsing Remitting Multiple Sclerosis: How Real-World Evidence Compares With Randomized Clinical Trials?,” Expert Review of Neurotherapeutics 21, no. 1 (2021): 21–34.
- E. Portaccio, A. Bellinvia, M. Fonderico, et al., “Progression Is Independent of Relapse Activity in Early Multiple Sclerosis: A Real-Life Cohort Study,” Brain 145, no. 8 (2022): 2796–2805.
- M. Filippi, R. Danesi, T. Derfuss, et al., “Early and Unrestricted Access to High-Efficacy Disease-Modifying Therapies: A Consensus to Optimize Benefits for People Living With Multiple Sclerosis,” Journal of Neurology 269, no. 3 (2022): 1670–1677.
- M. Filippi, M. P. Amato, D. Centonze, et al., “Early Use of High Efficacy Disease-Modifying Therapies Makes the Difference in People With Multiple Sclerosis: An Expert Opinion,” Journal of Neurology 269, no. 10 (2022): 5382–5394.
- A. Morgan, E. Tallantyre, and D. Ontaneda, “The Benefits and Risks of Escalation Versus Early Highly Effective Treatment in Patients With Multiple Sclerosis,” Expert Review of Neurotherapeutics 23, no. 5 (2023): 433–444.
- P. Iaffaldano, G. Lucisano, and T. Guerra, “Early Intensive Versus Escalation Approach: Ten-Year Impact on Disability in Relapsing Multiple Sclerosis,” Annals of Clinical and Translational Neurology (2025). doi:10.1002/acn3.70131.
- M. Trojano, R. Bergamaschi, M. P. Amato, et al., “The Italian Multiple Sclerosis Register,” Neurological Sciences 40, no. 1 (2019): 155–16
- P. Iaffaldano, G. Lucisano, T. Guerra, et al., “A Comparison of Natalizumab and Ocrelizumab on Disease Progression in Multiple Sclerosis,” Annals of Clinical Translational Neurology 11, no. 8 (2024): 2008–2015.
- M. Simone, G. Lucisano, T. Guerra, et al., “Disability Trajectories by Progression Independent of Relapse Activity Status Differ in Pediatric, Adult and Late-Onset Multiple Sclerosis,” Journal of Neurology 271, no. 10 (2024): 6782–6790.
- T. Spelman, A. Glaser, and J. Hilert, “Immediate High-Efficacy Treatment in Multiple Sclerosis Is Associated With Long-Term Reduction in Progression Independent of Relapse Activity (PIRA) Compared to Low-Moderate Efficacy Treatment – A Swedish MS Registry Study,” Multiple Sclerosis Journal 30, no. 3S (2024): 651.